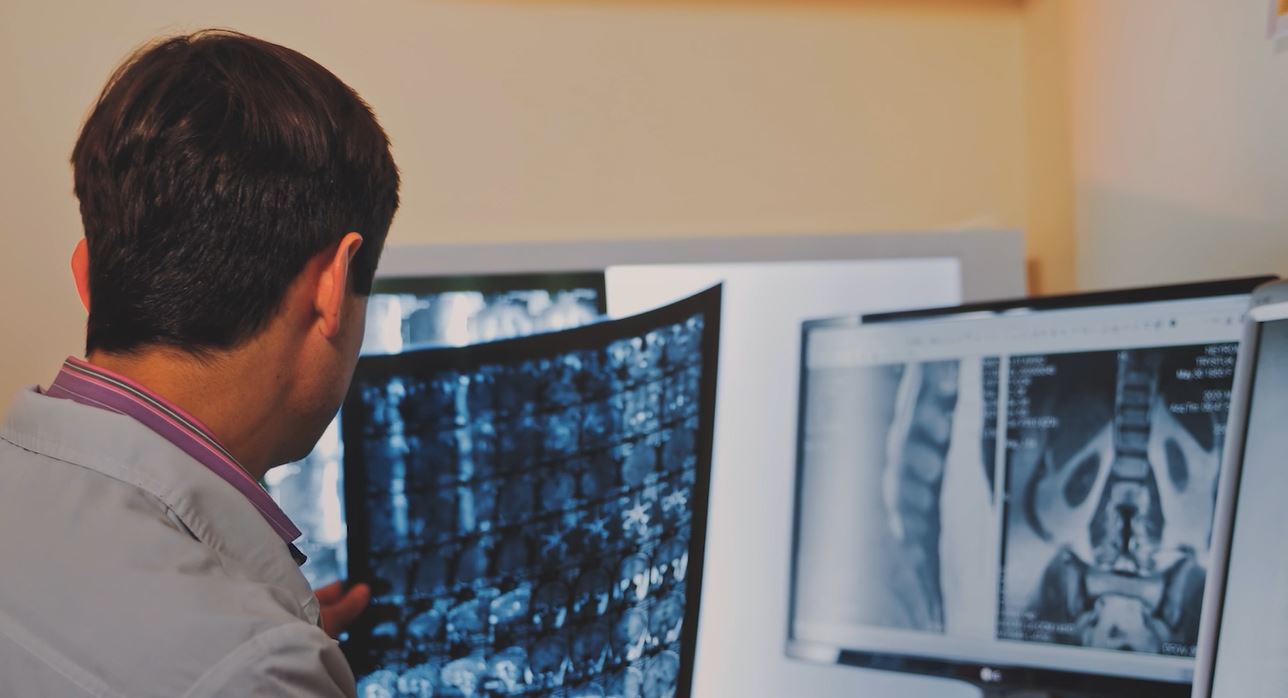
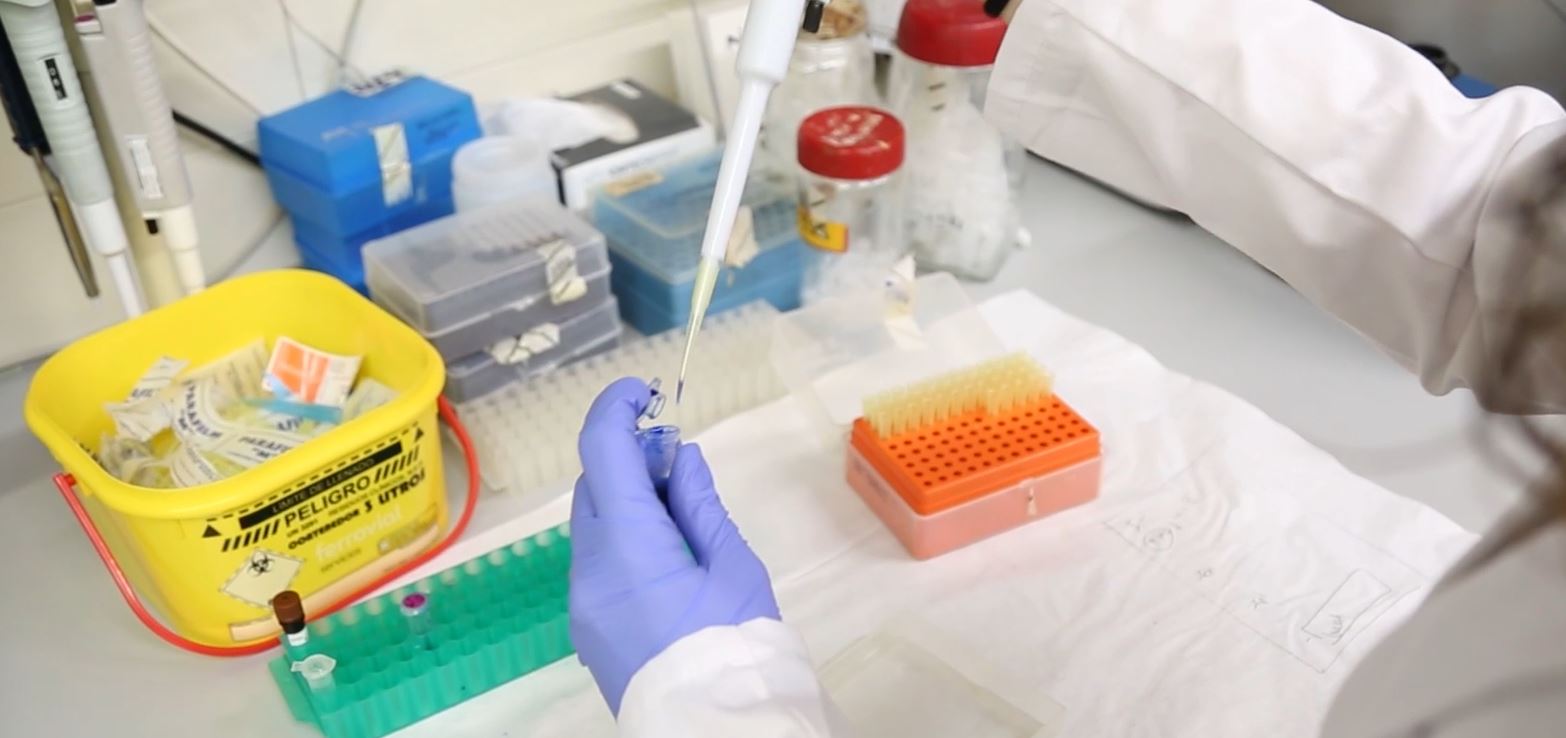
Monitor/a d'assajos clínics
Altres denominacions
Clinical Research Associate (CRA)
Descripció
El procés d'aprovació d'un nou medicament per a l'ús humà és complex i de llarga durada. Després de la recerca preclínica (in vitro i amb animals), un nou medicament es prova amb humans durant un assaig clínic a través d'una metodologia que distingeix tres fases, fins arribar a l'estudi i seguiment del fàrmac després de la seva comercialització o quarta fase. Normalment, tot el procés implica pel cap baix a unes 3.000 persones, dura entre cinc i deu anys (tot i que pot variar molt), i pot tenir un cost total entre 300 i 500 milions d'euros. Per aprovar-lo, cal presentar tota la documentació científica pel que fa als protocols seguits i als resultats obtinguts.
El/la monitor/a d'assajos clínics o clinical research associate és un/a cap de projecte que es responsabilitza de les pràctiques clíniques d'un assaig per a l'aprovació d'un medicament, i n'assegura la conformitat amb els requisits de l'agència reguladora. Treballa en empreses farmacèutiques o en CROs (Contract Research Organizations) que s'ofereixen per fer assajos clínics per a la indústria farmacèutica. Normalment, l'assaig clínic es reparteix entre diversos centres de diferents països.
Tasques
- Participa en el desenvolupament del pla clínic total, supervisa el desenvolupament i la revisió de protocols d'assajos clínics que hagin de complir les exigències de les agències reguladores i col·labora en l'organització dels plans d'anàlisis estadístiques.
- S'encarrega de la monitorització dels assajos clínics, coordina el seguiment científic, centralitza tota la informació i informa a tots els/les investigadors/es sobre l'evolució de l'assaig. Treballa sota normes de BPC (Bones Pràctiques clíniques).
- Participa en la identificació i selecció de centres clínics i d'investigadors/es, nacionals i internacionals, que han de complir unes qualificacions i experiència determinades.
- Proporciona als/a les investigadors/es clínics/ques tota la informació clínica, farmacològica i toxicològica rellevant sobre el producte estudiat per fer una planificació correcta i dur a terme l'assaig, a més de la informació essencial que estigui al seu abast durant l'assaig.
- S'assegura de la traçabilitat de la medicació entregada, la recollida de la no administrada i de qualsevol incidència relacionada amb la mateixa.
- Organitza reunions amb tots els/les participants de clíniques, agències reguladores i investigadors/es, per tal de vigilar el seguiment de l'assaig clínic, identificar problemes i resoldre les desviacions que es donin en el protocol.
- Assegura la transmissió apropiada de les dades clíniques sobre el cas a l'agència reguladora.
- Fa el seguiment i control dels/de les col·laboradors/es designats/des en cada projecte.
- Prepara i manté actualitzat l'arxiu de l'estudi sota normativa BPC.










 | català | principiant
| català | principiant | català | avançat
| català | avançat
 Obrir
Obrir | català | principiant
| català | principiant